Αντικείμενο και στόχοι του έργου.
Η έκθεση ανθρώπινων ιστών και κυττάρων σε μειωμένη συγκέντρωση οξυγόνου (υποξία) παρατηρείται σε φυσιολογικές και παθολογικές περιπτώσεις, που περιλαμβάνουν την εμβρυογένεση, την ανάπτυξη, την πνευμονική δυσλειτουργία, τις ισχαιμίες, τη φλεγμονή και τον καρκίνο. Τα κύτταρα και οι οργανισμοί που εκτίθενται σε υποξία αποκρίνονται αλλάζοντας την έκφραση ενός μεγάλου αριθμού γονιδίων προκειμένου να προσαρμοστούν και να επιβιώσουν. Απαραίτητοι σε αυτή την απόκριση είναι οι επαγόμενοι από την υποξία παράγοντες ΗΙF-1 και HIF-2, οι οποίοι ρυθμίζουν την έκφραση των περισσότερων γονιδίων στόχων της υποξίας, όπως αυτών που εμπλέκονται στην αγγειογένεση, το μεταβολισμό, την ερυθροποίηση, την κυτταρική επιβίωση/απόπτωση, τη μετανάστευση και άλλες ιστοειδικές λειτουργίες, συμπεριλαμβανομένης της φλεγμονής και της ίνωσης.
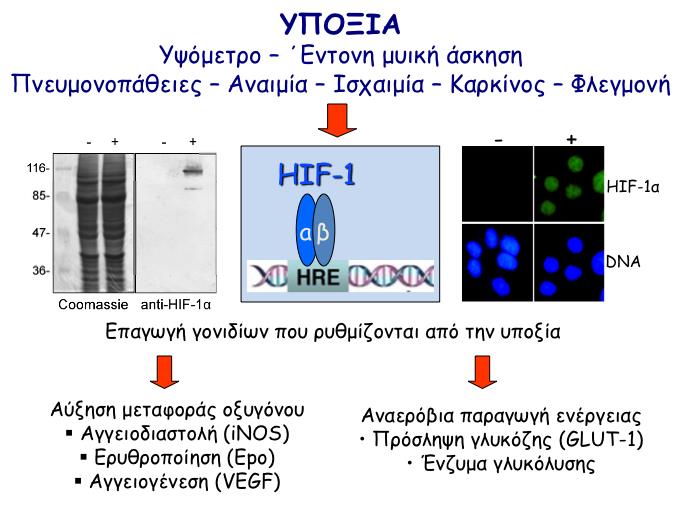
Τα επίπεδα οξυγόνου καθορίζουν τη δραστικότητα των HIF μέσω της υδροξυλίωσης των HIF-α ρυθμιστικών υπομονάδων τους. Ωστόσο, στον ιστοειδικό, διαφορικό ή ειδικό για τις διαφορετικές ισομορφές και χωρο-χρονικό έλεγχο των HIF στον καρκίνο, εμπλέκονται μοριακοί μηχανισμοί, που δεν εξαρτώνται από το οξυγόνο, η κατανόηση των οποίων απαιτεί περαιτέρω διερεύνηση και αποτελεί τον πρώτο στόχο του παρόντος έργου.
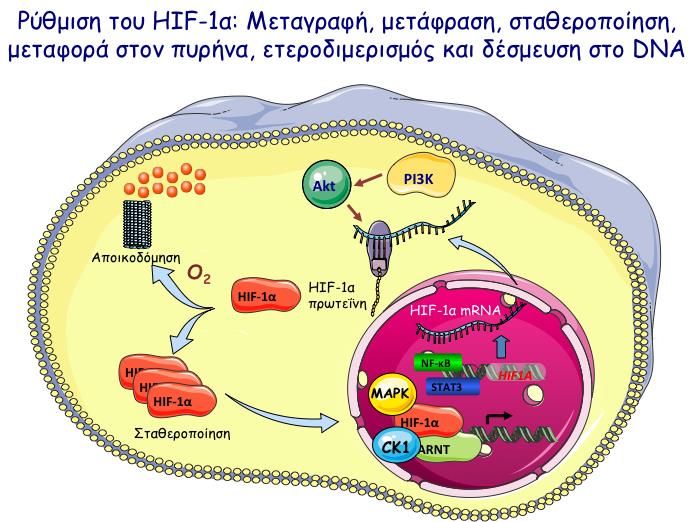
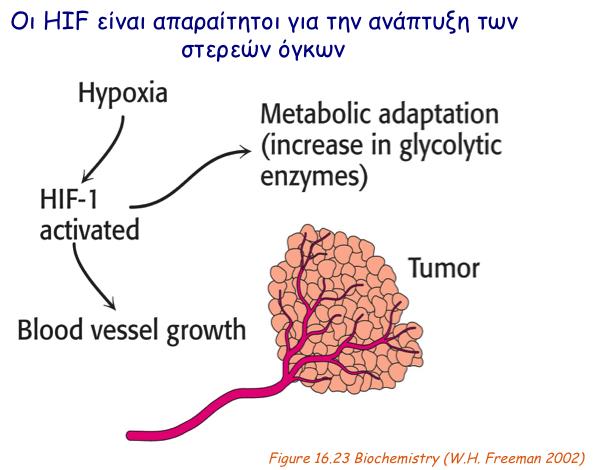
Όσον αφορά τον καρκίνο, κοινό χαρακτηριστικό πολλών συμπαγών όγκων είναι η ανάπτυξη υποξικών περιοχών, εξαιτίας του αυξημένου κυτταρικού πολλαπλασιασμού και της περιορισμένης παροχής αίματος. Η υποξία μπορεί να προάγει την ανάπτυξη όγκων διευκολύνοντας την αγγειογένεση και τη μεταβολική προσαρμογή των καρκινικών κυττάρων. Καθώς οι HIF είναι κύριοι παράγοντες της προσαρμογής των καρκινικών κυττάρων στη στέρηση οξυγόνου, οι HIF-α υπομονάδες τους υπερεκφράζονται σε πολλούς καρκίνους, σχετίζονται με κακή πρόγνωση και γι’ αυτό αποτελούν ελκυστικούς θεραπευτικούς στόχους. Η ανάπτυξη καινοτόμων παραγόντων που θα έχουν την ιδιότητα να σκοτώνουν τα καρκινικά κύτταρα στοχεύοντας ειδικά τους HIF είναι ο δεύτερος στόχος του παρόντος έργου.
Οι HIF επάγονται επίσης από προ-φλεγμονώδεις παράγοντες και πιθανόν εμπλέκονται στην ιστική αναδιαμόρφωση και ίνωση που παρατηρούνται στις χρόνιες φλεγμονώδεις διαταραχές. Πρόσφατες μελέτες με διαγονιδιακά ποντίκια, υποδεικνύουν ότι η ενεργοποίηση των HIF μπορεί να προκαλέσει συσσώρευση λίπους στο ήπαρ και στεατοηπατίτιδα, συμβάλλοντας στην ανάπτυξη μεταβολικών διαταραχών, κίρρωσης και ηπατοκυτταρικού καρκινώματος (HCC). Τα ηπατοκύτταρα εκφράζουν HIF-1α και HIF-2α, ωστόσο ο ρόλος του καθενός τους στο μεταβολισμό και στην παθολογία του ήπατος παραμένει σε μεγάλο βαθμό άγνωστος, και αποτελεί, για το λόγο αυτό, τον τρίτο στόχο του παρόντος έργου.
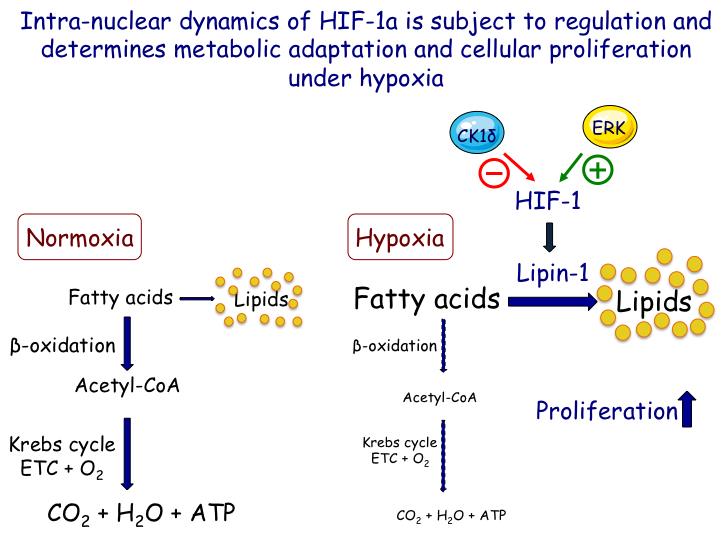
Η παρούσα έρευνα έχει στόχο την κατανόηση της οξυγονο-ανεξάρτητης ρύθμισης των HIF-1 και HIF-2 και την ανάπτυξη μοριακών μεθόδων για τη διερεύνηση και τροποποίηση της δράσης τους, ιδιαίτερα όσον αφορά το μεταβολισμό των κυττάρων του ήπατος, τη φλεγμονή και την καρκινογένεση. Τα αναμενόμενα αποτελέσματα θα εκπληρώσουν τους ακόλουθους τρεις στόχους:
Στόχος 1: Διαλεύκανση του ρόλου της φωσφορυλίωσης και των πρωτεϊνικών αλληλεπιδράσεων στη χρονική, χωρική και διαφορική ρύθμιση της ενεργοποίησης και δράσης των ισομορφών του HIF.
Στόχος 2: Ανάπτυξη ειδικών αναστολέων του HIF-1, οι οποίοι θα χρησιμοποιηθούν σε νέες στρατηγικές αντικαρκινικής και αντιφλεγμονώδους θεραπείας.
Στόχος 3: Διευκρίνιση του ρόλου των ισομορφών του HIF στον ηπατικό μεταβολισμό των λιπιδίων και στη φλεγμονή.
Συνοπτικά, tο έργο έχει στόχο να παράγει νέες γνώσεις σχετικές με τους μοριακούς μηχανισμούς που διέπουν την κυτταρική απόκριση στην υποξία και την δυσπροσαρμοστική συμμετοχή τους στην παθογένεια του καρκίνου, της φλεγμονής και συχνών μεταβολικών διαταραχών όπως το λιπώδες ήπαρ. Τα αποτελέσματα που παράγονται και τα αντιδραστήρια που αναπτύσσονται είναι δυνατόν να οδηγήσουν στην ανάπτυξη νέων στρατηγικών για την αποτελεσματική αντιμετώπιση των παραπάνω ασθενειών.


